Bis März 2023 wurden 11 medizinische Exoskelette von der US-amerikanischen FDA für das Gehen, die Gangunterstützung und die körperliche Rehabilitation zugelassen. Die FDA klassifiziert medizinisch angetriebene Exoskelette als Geräte der Klasse II, Code PHL, mit der genauen Definition wie folgt: „Ein angetriebenes Exoskelett ist ein verschreibungspflichtiges Gerät, das aus einer externen, angetriebenen, motorisierten Orthese besteht, die über dem gelähmten oder geschwächten Unterleib einer Person platziert wird Extremität(en) für medizinische Zwecke.“
Die 11 medizinischen Exoskelette sind in keiner bestimmten Reihenfolge:
- Keeogo Dermoskeleton System von B-Temia, angetriebenes Knie-Exoskelett
- HAL für medizinische Zwecke (Typ der unteren Extremitäten) von CYBERDYNE, angetriebenes Hüft-Knie-Exoskelett
- EksoNR von Ekso Bionics angetriebenes Hüft-Knie-Exoskelett
- ExoAtlet-II von ExoAtlet Asia, ebenfalls ein angetriebenes Hüft-Knie-Exoskelett
- Honda Walking Assist Device, Honda Motor Company, angetriebenes Hüft-Exoskelett
- Indego, offiziell von der Parker-Hannifin Corporation, kürzlich von EksoBionics übernommen, angetriebenes Hüft-Knie-Exoskelett
- ReWalk von ReWalk Robotics, angetriebenes Hüft-Knie-Exoskelett
- ReWalk ReStore von ReWalk Robotics, motorisierter Knöchel-Exosuit
- GEMS-H von Samsung Electronics, angetriebenes Hüft-Exoskelett
- Phoenix von Ottobock, offiziell suitX (was selbst offiziell US Bionics war), ist ein angetriebenes Hüft-Exoskelett mit passiver Knieunterstützung
- Atalante von Wandercraft SAS angetriebenes Hüft-Knie-Knöchel-Exoskelett
Ab März 2023 ist nur das ReWalk-Exoskelett von der FDA für die Verwendung mit Treppen und Bordsteinen zugelassen. Nur ReWalk Personal und Indego sind für den privaten oder privaten Gebrauch zugelassen. Alle Geräte können in der Umgebung eines Rehabilitationszentrums verwendet werden. Der Atalante ist das einzige selbstausgleichende Exoskelett, das von der FDA zugelassen ist (obwohl der REX bald in die Liste aufgenommen werden könnte). Die restlichen Geräte verfügen entweder über optionale oder erforderliche zusätzliche Mobilitätshilfen wie Krücken oder eine Gehhilfe. Es gibt mehrere Geräte, wie das Atalante, die möglicherweise von Jugendlichen verwendet werden können (aber es gibt keine pädiatrischen Exoskelette auf dieser Liste). Alle Bediener müssen vor der Verwendung der Exoskelette ein Schulungsprogramm absolvieren.
Einige der von der FDA zugelassenen angetriebenen Exoskelette haben spezielle Absturzsicherungs- und Minderungsüberlegungen, insbesondere:
- Atalante: muss in Kombination mit einem Sicherheitsgeländer verwendet werden.
- ReWalk muss mit Krücken verwendet werden. Der Indego, der ExoAtlet-II (und vermutlich der Phoenix) sollten mit Krücken oder einem Rollator verwendet werden, während der EksoNR mit Krücken, einem Rollator oder einem Gehstock verwendet werden kann.
- Der HAL für medizinische Zwecke muss an einem Körpergewichtsstützsystem befestigt werden (normalerweise über Kopf).
- Alle Versionen des ReWalk und des Indego mit Ausnahme der Versionen für den Heimgebrauch wurden nur für die Verwendung unter der Aufsicht eines ausgebildeten medizinischen Fachpersonals freigegeben.
Der beabsichtigte Ese-Fall für die von der FDA zugelassenen angetriebenen Exoskelette soll Patienten/Benutzern beim Gehen helfen mit:
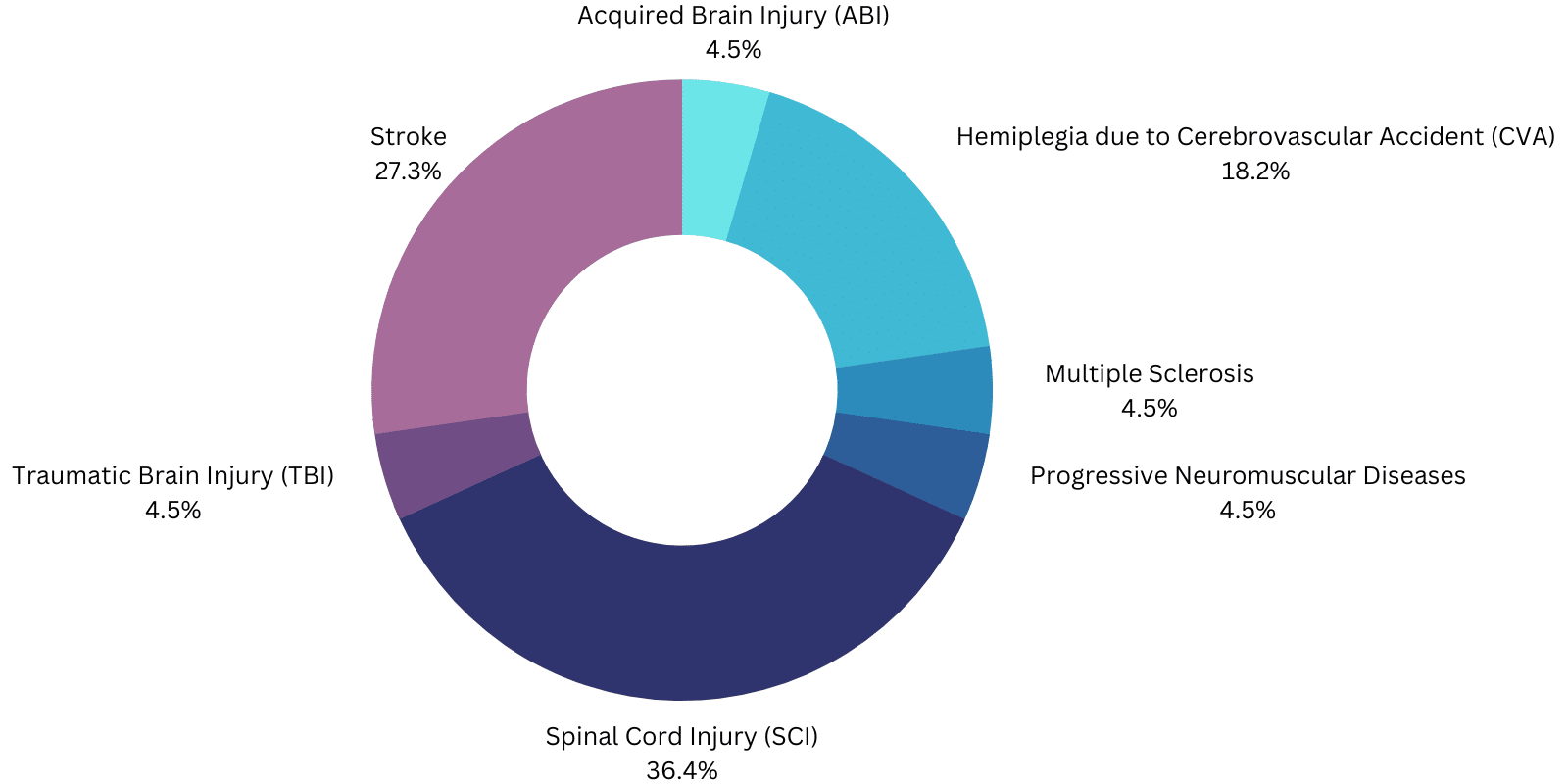
- ExoAtlet-II dient der funktionellen Rehabilitation von Personen unter Aufsicht eines ausgebildeten Physiotherapeuten mit einer motorischen Funktion der oberen Extremitäten von mindestens 4/5 in beiden Armen, die Rückenmarksverletzungen (SCI) T4 bis L5 oder C7 bis T3 (ASIA D ).
- Phoenix: Rückenmarksverletzung (SCI) der Ebene T4-L5.
- Atalante: Hemiplegie aufgrund eines zerebrovaskulären Unfalls (CVA).
- GEMS-H: Personen mit Schlaganfall, die Gangdefizite haben und Ganggeschwindigkeiten von mindestens 0,4 m/s aufweisen und in der Lage sind, mindestens 10 Meter mit Hilfe von maximal einer Person zu gehen.
- ReWalk: SCI T7 bis L5 für den persönlichen Gebrauch unter ständiger Überwachung oder SCI T4 bis T6 zur körperlichen Rehabilitation in einer speziellen Einrichtung.
- ReWalk Restore: sollte „verwendet werden, um ambulante Funktionen in Rehabilitationseinrichtungen unter der Aufsicht eines ausgebildeten Therapeuten für Menschen mit Hemiplegie/Hemiparese aufgrund eines Schlaganfalls zu unterstützen, die mindestens 1,5 m (5 Fuß) mit nicht mehr als minimaler bis mäßiger Unterstützung gehen können .“
- Indego: Ambulante Hilfe für SCI-Stufen T3 bis L5 für den persönlichen Gebrauch mit Überwachung und SCI der Stufen C7 bis L5 in Rehabilitationseinrichtungen oder Hemiplegie aufgrund von CVA mit motorischer Funktion 4/5 in mindestens einer oberen Extremität.
- Honda Walking Assist: „Personen mit Schlaganfall, die Gangdefizite haben und Ganggeschwindigkeiten von mindestens 0,4 m/s aufweisen und in der Lage sind, mindestens 10 Meter mit Hilfe von maximal einer Person zu gehen“ in Rehabilitationseinrichtungen.
- EksoNR: „Das EksoNRm soll ambulante Funktionen in Rehabilitationseinrichtungen unter der Aufsicht eines ausgebildeten Physiotherapeuten für die folgenden Bevölkerungsgruppen ausführen:
- Personen mit Multipler Sklerose (motorische Funktion der oberen Extremität von mindestens 4/5 in mindestens einem Arm).
- Personen mit erworbener Hirnverletzung, einschließlich traumatischer Hirnverletzung und Schlaganfall (motorische Funktion der oberen Extremität von mindestens 4/5 in mindestens einem Arm).
- Personen mit Rückenmarksverletzungen der Ebenen T4 bis L5 (motorische Funktion der oberen Extremität von mindestens 4/5 in beiden Armen).
- Personen mit Rückenmarksverletzungen auf den Ebenen C7 bis T3 (ASIA D mit einer motorischen Funktion der oberen Extremitäten von mindestens 4/5 in beiden Armen).
Gemeldete Größen- und Gewichtsbeschränkungen für Benutzer:
| Gerät: | Höhenbereich des Benutzers | Gewichtsbereich des Benutzers |
| GEMS-H | 1,55m bis 1,91m | 45 bis 100 kg |
| Atalanta | 1,60 bis 1,90 cm | bis 90 kg |
| Phönix | 1,60m bis 1,87m | bis 91 kg |
| ReWalk | 1,60m bis 1,90m | bis 100 kg |
| ReWalk-Wiederherstellung | 1,42m bis 1,92m | bis 120 kg |
| Ich brauche | 1,50m bis 1,90m | bis 113 kg |
| Honda Gehhilfe | 1,4m bis 2,0m | bis 100 kg |
| ExoAthlete-II | 1,60m bis 1,90m | bis 100 kg |
| ExoNR | 1,58m bis 1,88m | bis 100 kg |
| HAL für medizinische Zwecke | 1,50m bis 1,90m | 40 bis 100 Kilo |
| Keegos Dermoskelett-System | 1,52m bis 1,88m | bis 130 kg |
Wenn Sie Fehler sehen oder einen Artikel zu einem bestimmten Thema wünschen, zögern Sie nicht, uns über das ExR-Kontaktformular zu kontaktieren . Ausgewähltes Bild (oben): Vorführung des Ekso GT durch Shane Mosko und die Physiotherapeutin Jenn Macievich im Hauptquartier von Ekso Bionics, Richmond, 2016 (Hintergrund entfernt).
Źródło:
- Produktklassifizierung, FDA, Zugriff März 2023, Link
- Palermo AE, Maher JL, Baunsgaard CB, Nash MS. Klinikorientierter Überblick über die Verwendung eines bionischen Exoskeletts nach einer Rückenmarksverletzung. Top Spinal Cord Inj Rehabil. Sommer 2017;23(3):234-244. doi: 10.1310/sci2303-234. PMID: 29339899; PMC-ID: PMC5562031.
- Evaluation of Safety and Performance of the Atalante System With Patients With Lower Limb
- Paralysis, NIH, 2018, Link
Ursprungsquelle: Vorgesehene Verwendung der 11 von der FDA zugelassenen medizinischen Exoskelette im Medical Exoskeleton Report 2023
